借用细胞“自噬”降解病毒蛋白——定量合成生物学全国重点实验室司龙龙和施小山团队建立减毒活疫苗设计新方法AUTOTAR
流感病毒是长期影响全球公共卫生的重要呼吸道病原体,其传播范围广、变异速度快,每年可造成大量感染与死亡。疫苗接种是预防流感最经济有效的手段之一。其中,减毒活疫苗是一类重要的疫苗研发方法,通过限制病毒复制实现毒力减弱,在降低致病性的同时,可保留病毒完整抗原与天然构象,并激发黏膜免疫、体液免疫和细胞免疫应答。然而,如何在安全性与免疫效力之间达到精准平衡,仍是减毒活疫苗研发的核心科学难题:减毒不足可能带来潜在安全风险,减毒过度则可能降低免疫原性。
近日,中国科学院深圳先进技术研究院定量合成生物学全国重点实验室、合成生物学研究所司龙龙、施小山课题组在国际学术期刊Nature Communications发表了题为《Generation of an autophagy targeting influenza A virus as live attenuated vaccine》的最新研究成果。该研究建立并验证了基于细胞自噬机制的减毒活疫苗设计体系(AUTOTAR),通过利用人体细胞天然的蛋白质降解通路,实现了对流感病毒的条件性精准减毒,为平衡疫苗安全性、免疫原性与可量产性提供了新的技术路径。

文章上线截图
原文链接:https://www.nature.com/articles/s41467-026-72426-4
随着病毒持续变异以及防控需求的不断提升,广谱、安全、持久、快速迭代的疫苗技术仍是领域内重点探索方向。减毒活疫苗因能够模拟自然感染、激活全面免疫应答而具备独特优势,在此背景下,发展新型、精准可控的病毒减毒技术,具有重要的科学价值与应用潜力。
细胞自噬是真核生物体内高度保守且普遍存在的生理性降解通路,是细胞维持自身内环境稳态的重要方式。在正常生理条件下,细胞可通过自噬通路识别胞内受损冗余、错误折叠的蛋白以及异常细胞器;经由自噬体完成包裹分选后,转运至溶酶体进行降解与物质循环利用,进而清除胞内异常组分、维系细胞正常代谢功能。这一降解过程依赖于ATG8家族蛋白识别特异性靶向基序,能够实现目标蛋白的选择性降解,且不干扰细胞正常生理运转,具备良好的特异性、稳定性与安全性。因此,研究团队提出一个科学假设:如果将自噬识别信号精准引入病毒蛋白,就可能在正常细胞中触发病毒蛋白的选择性降解,从而实现病毒减毒;而在工程细胞中移除该信号,则可支持病毒高效复制。基于这一思路,团队设计并构建了可条件性去除的自噬靶向标签,探索其在流感病毒上的应用(图1)。
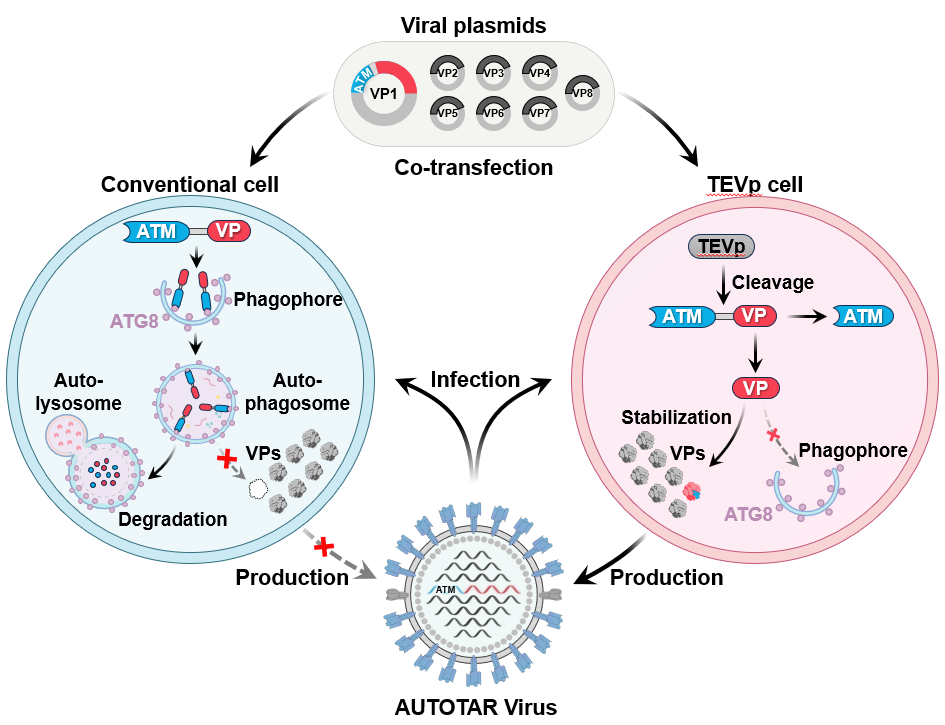
图1. AUTOTAR疫苗的设计思路
团队首先对流感病毒多种蛋白进行系统筛选,最终确定在NS1蛋白N端引入自噬靶向基序(ATM),并通过TEV酶切位点实现标签的可控切除。
在体外细胞模型中,改造后的病毒在常规细胞中复制能力显著降低,表现为高度减毒;在表达蛋白酶的工程细胞中,自噬标签可被高效切除,病毒恢复高效复制能力(图2)。进一步机制实验证实,病毒蛋白的降解依赖自噬通路,而非蛋白酶体通路,为这一减毒策略的可靠性提供了机制支撑。
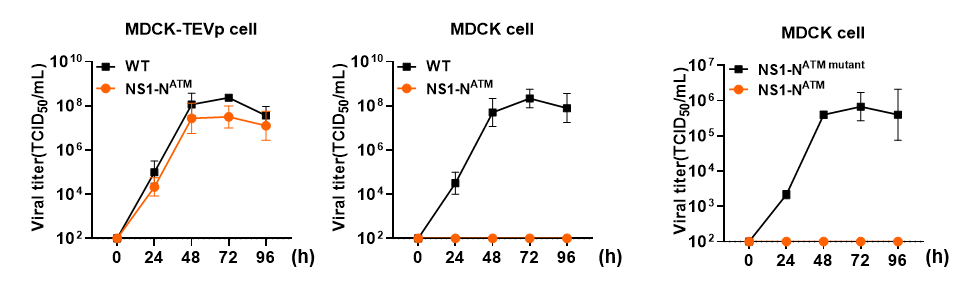
图2. AUTOTAR疫苗体外复制动力学特征
在小鼠模型中,团队对疫苗株进行了系统评价。与野生型流感病毒相比,接种相同剂量的 AUTOTAR 疫苗后,小鼠未出现体重下降、肺部损伤及死亡,体内也未检出具有传播风险的活病毒,且经过连续传代后,病毒基因组保持稳定,未出现病毒突变迹象,充分验证了AUTOTAR疫苗株在小鼠模型中的安全性(图3)。
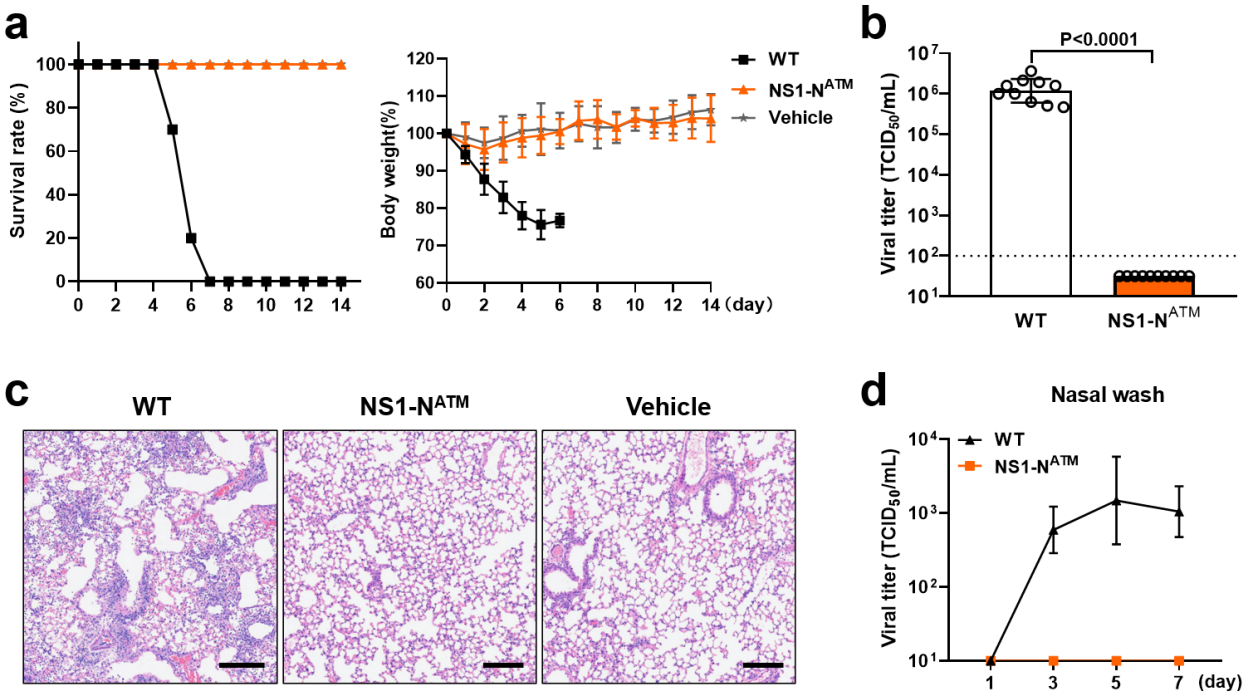
图3. 小鼠体内安全性验证
动物免疫实验显示,单次鼻喷接种AUTOTAR疫苗可有效诱导产生体液免疫、黏膜免疫与细胞免疫应答(图4)。
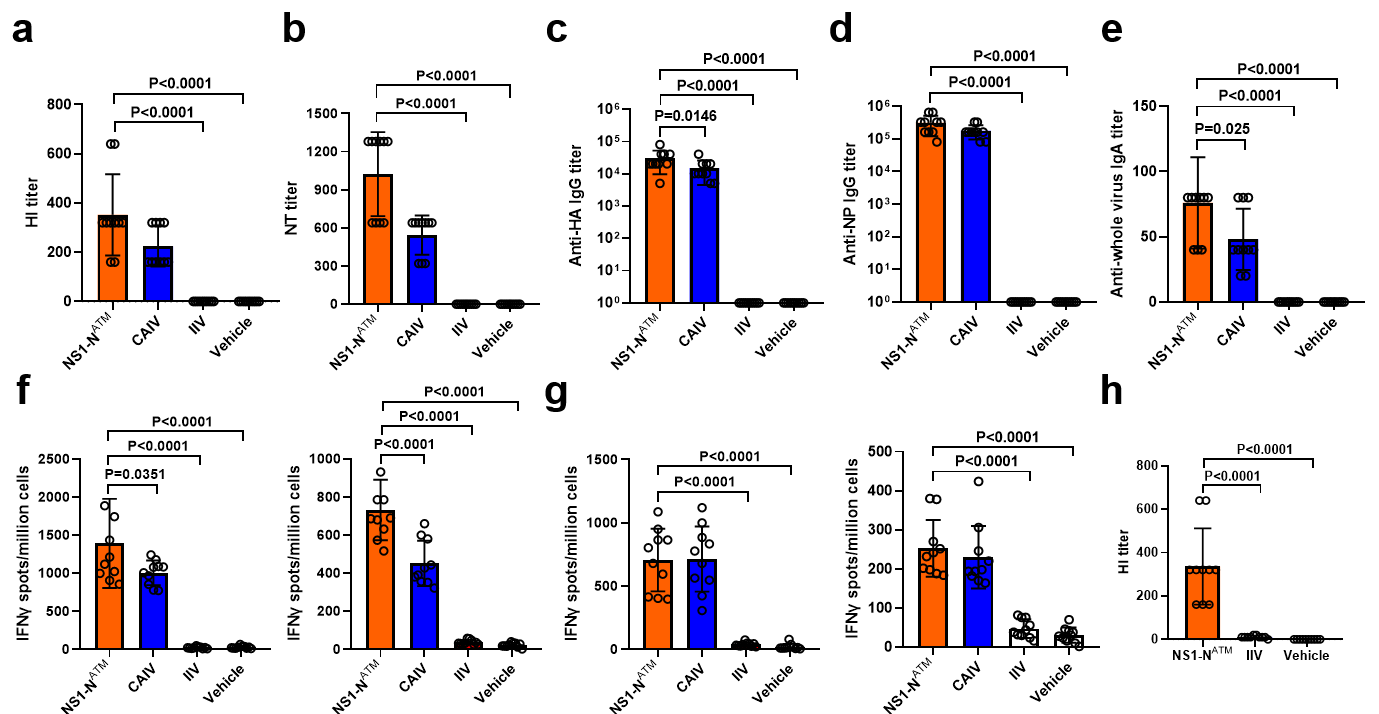
图4. AUTOTAR疫苗的免疫原性评价
AUTOTAR疫苗对同型流感病毒攻击提供完全保护,并对不同亚型毒株展现出良好的交叉保护潜力(图5)。
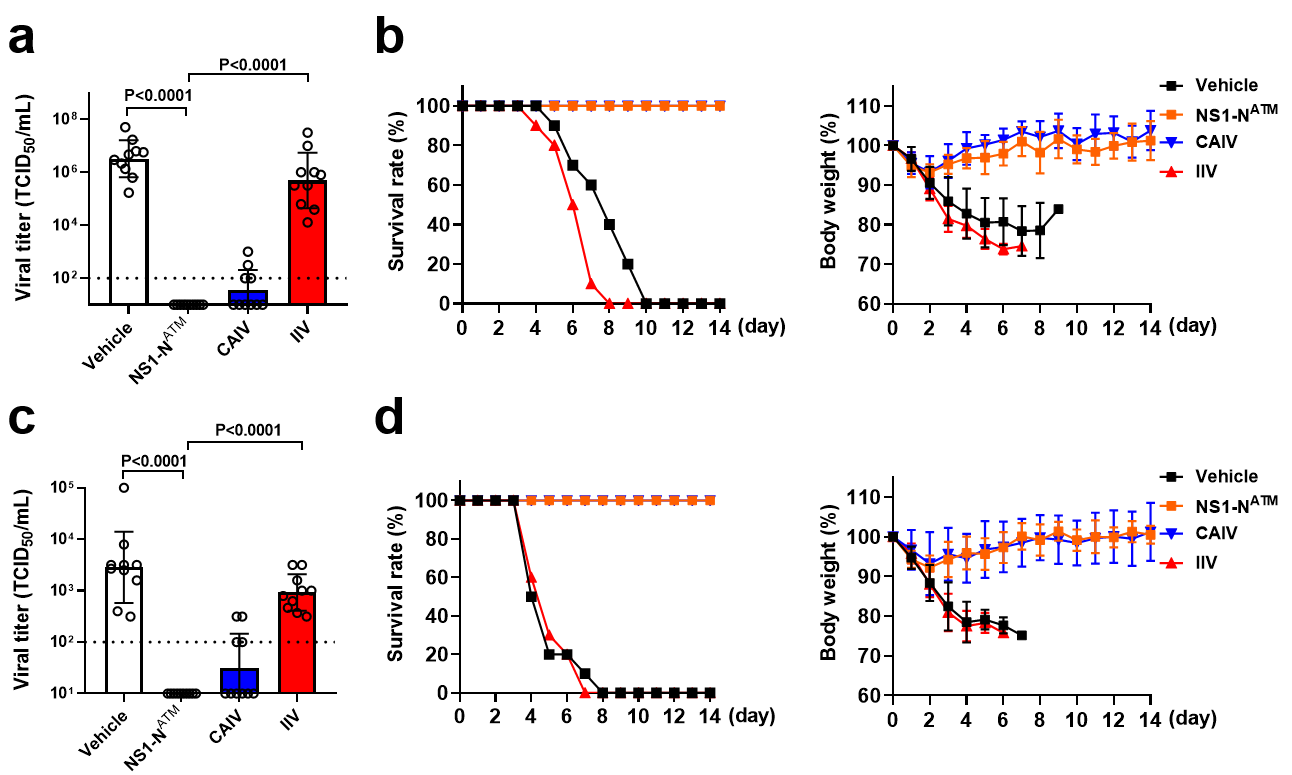
图5. AUTOTAR疫苗的交叉免疫保护效果
该研究将细胞自噬机制系统应用于减毒活疫苗设计,验证了 “自噬靶向调控病毒复制” 这一思路的可行性,丰富了基于蛋白质降解的疫苗设计理论与技术体系。随着相关技术的不断完善,AUTOTAR技术平台有望拓展应用于更多病毒类疫苗研发,为新一代疫苗技术创新、传染病防控体系完善与公共卫生安全保障提供新的技术思路与有力支撑。目前,该技术完成了实验室概念验证,后续仍需通过系统性的大动物实验评价,以全面验证疫苗的安全性、免疫原性与保护效力。同时,该技术的通用性仍需在更多病毒模型中进行拓展验证,以评估其在不同病原体背景下的适用性与稳定性。
中国科学院深圳先进技术研究院为第一单位和通讯单位。中国科学院深圳先进技术研究院定量合成生物学全国重点实验室、合成生物学研究所司龙龙、施小山研究员为共同通讯作者,郝嘉玮、王平博士为论文共同第一作者。该研究得到国家自然科学基金、国家重点研发计划以及深圳合成生物学创新研究院等项目支持。
