Curr. Opin. Biotechnol. | 空间酶组装策略赋能微生物药物合成
微生物合成凭借可持续、高效率的优势,已成为重要的药物生产方式。然而,在微生物细胞工厂中异源表达合成途径时,经常面临中间物扩散、代谢通量竞争、细胞毒性中间体积累等问题。大自然中,很多途径酶受到精准空间组织调控,从而具有高效性和专一性。受到这种空间调控方式的启发,研究人员开发了人工空间酶组装工具来提升微生物药物合成效率。
近日,中国科学院深圳先进技术研究院定量合成生物学国家重点实验室、合成生物学研究所马田副研究员作为通讯作者,在国际权威期刊Current Opinion in Biotechnology发表综述文章。该文章系统总结了空间酶组装在微生物药物合成中的最新研究进展,全面梳理了四大核心组装策略的设计原理、特性优势与应用场景,深入剖析领域现存挑战,并提出未来发展方向,为高效、可持续的生物制造提供了全新的设计思路与实践参考。

文章上线截图
原文链接:https://doi.org/10.1016/j.copbio.2026.103475
四大核心策略:解锁酶空间组装的多元技术路径
1.理性设计连接肽介导多酶组装
通过理性设计连接肽将酶直接融合,可以缩短酶之间的距离、优化代谢物递送,提高催化效率,将多酶空间优化从经验试错推向理性设计。
2.肽-蛋白互作结构域介导多酶组装
依托肽-肽、肽-蛋白的特异性互作,可以实现酶的模块化组装,该类互作元件的多样性与正交性为复杂酶组装提供了可能。其中RIDD-RIAD、SpyTag / SpyCatcher、PKS对接结构域介导的关键酶组装显著提高类胡萝卜素、紫穗槐二烯、虾青素等的生物合成效率。
3.核酸支架介导多酶组装
DNA/RNA具有可编程特性,DNA/RNA支架介导的多酶组装可灵活调控组装酶的数量、顺序、化学计量比与间距。基于CRISPR/dCas的DNA/RNA支架系统,显著提高了组装酶的催化效率,为代谢通路的精细调控提供了新的可能。
4.自组装元件介导多酶组装
利用蛋白自组装特性形成天然聚集结构,实现酶的自发共定位。自组装元件CipB蛋白、固有无序蛋白(IDPs)介导的酶组装,显著提升叶黄素、诺卡酮、2'-岩藻糖基乳糖等的生物合成效率。
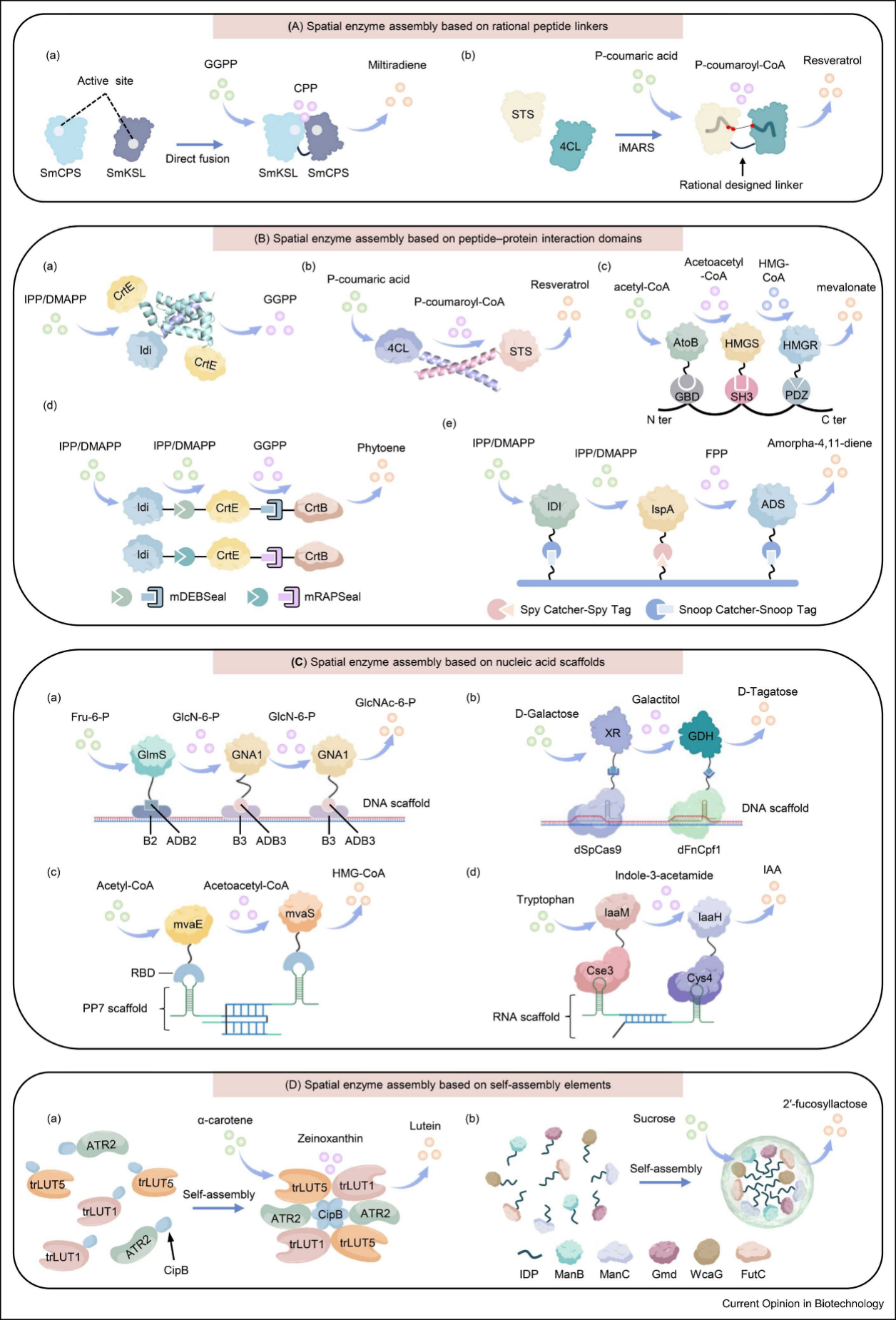
图 | 微生物药物生物合成的空间酶组装策略
机遇与挑战:空间酶组装技术的发展瓶颈
尽管空间酶组装技术已在抗肿瘤药物、抗疟药等多类药物合成中取得显著成效,但仍面临多重挑战:现有工具对酶的排列顺序、化学计量比、酶间距的精细调控有限;组装复合物在高温、极端pH、高底物浓度等工业发酵严苛条件下的稳定性与兼容性有待提升;涉及复杂的多酶装配,易给宿主细胞带来代谢负担等。
未来展望:合成生物学与AI融合
为突破瓶颈,未来研究将聚焦三方面:从天然超分子结构、极端微生物中挖掘新型组装模块;依托AlphaFold3、iMARS等工具,实现AI赋能的组装元件理性设计;整合AI设计模块与现有策略,开发更高效稳定的组装系统,推动微生物药物合成工业化升级,助力可持续生物制造。
该综述第一作者为中国科学院深圳先进技术研究院硕士生郑楚怡,马田副研究员为通讯作者。研究工作得到国家自然科学基金、广东省基础与应用基础研究基金、深圳市科技计划以及深圳合成生物学创新研究院等项目的资助。
