Science Advances | 当经典代谢酶“走进细胞核”:植物如何为黄酮代谢踩下“分子刹车”?
植物如何在复杂环境中精准调控自身代谢,一直是植物生物学领域的重要科学问题。尤其是苯丙烷代谢通路,它不仅决定植物的抗逆能力,也影响黄酮、木质素和水杨酸等关键代谢物的合成。然而,一个长期未解决的问题是:当黄酮等代谢物积累过多时,植物如何快速“踩刹车”,避免代谢过载?
近日,中国科学院深圳先进技术研究院定量合成生物学全国重点实验室、合成基因组学研究中心赵乔团队在国际权威期刊Science Advances发表研究成果。团队首次发现,苯丙烷通路关键酶Phenylalanine ammonia-lyase(PAL)不仅在细胞质中催化类黄酮合成的起始反应,还能通过磷酸化修饰进入细胞核,以双重机制精准调控黄酮类化合物的合成总量。这项研究颠覆了“PAL仅为胞质酶”的传统认知,提出植物通过调控酶的亚细胞定位,实现代谢与转录双重反馈调控的新机制。

文章上线截图
原文链接:https://www.science.org/doi/10.1126/sciadv.adz6970
当代谢酶进入细胞核:PAL的“第二身份”
PAL传统上被认为定位于细胞质,而本研究首次证实PAL不仅存在于胞质中,还可显著存在于细胞核中。该核定位具有动态可逆性:在UV-B辐射或高蔗糖处理诱导黄酮生物合成增强时,PAL在细胞核中富集;刺激解除后,其重新分布至胞质。该过程不依赖新蛋白合成,提示PAL通过快速、可逆的亚细胞定位重分配参与代谢调控。
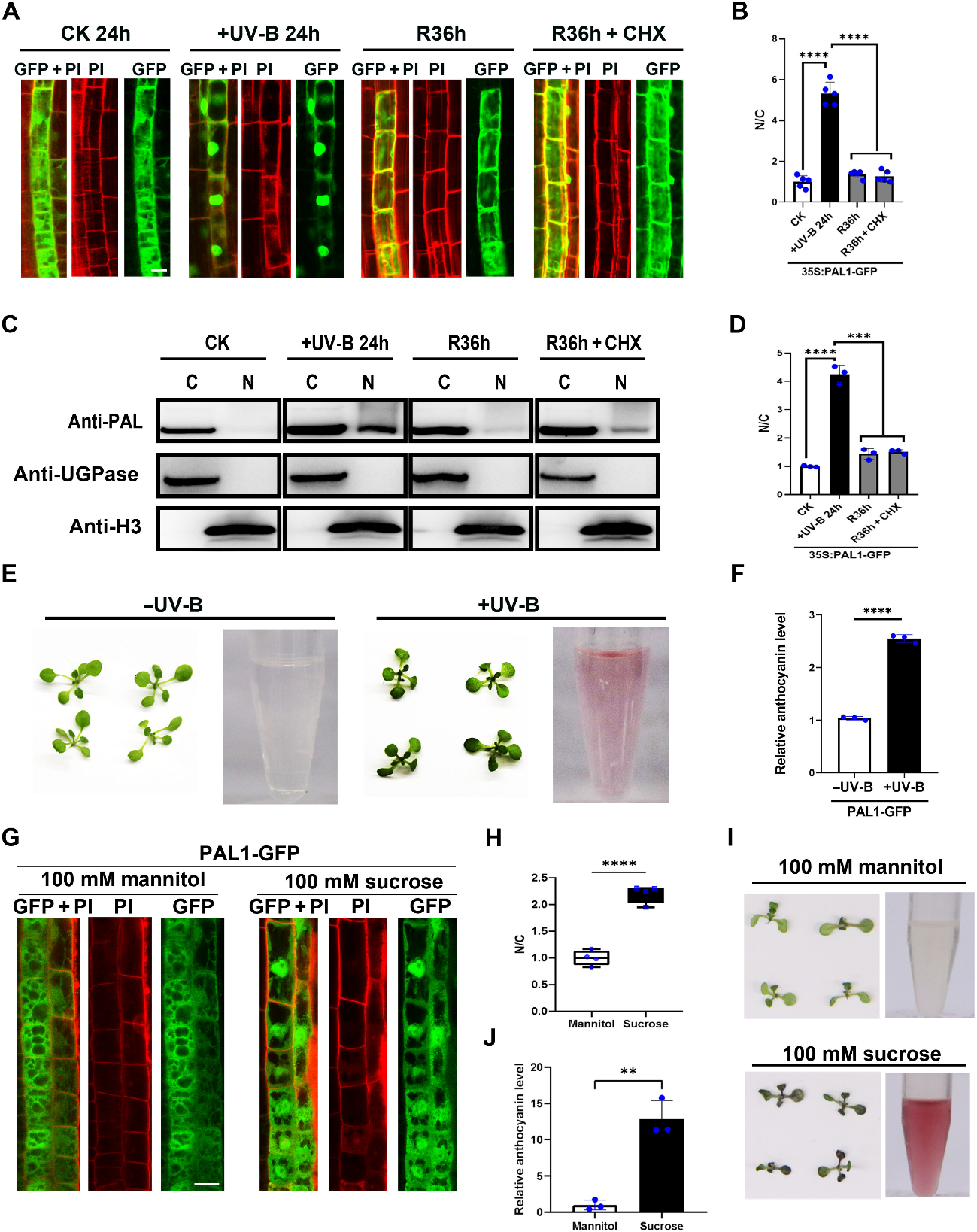
图1. PAL 蛋白的可逆定位
磷酸化开关:谁在推动PAL入核?
研究进一步发现,黄酮通路中间体Naringenin(NAR)可以诱导PAL发生磷酸化修饰。通过质谱分析,研究团队鉴定出关键磷酸化位点(S152、T153、S163)。当这些位点模拟持续磷酸化时,PAL持续定位于细胞核;当这些位点失去磷酸化能力时,PAL则无法响应NAR进入细胞核。这说明,磷酸化是PAL入核的分子开关。这也提示,植物体内可能存在一个尚未被鉴定的“黄酮信号感受-激酶模块”,负责感知代谢状态并驱动PAL转位。
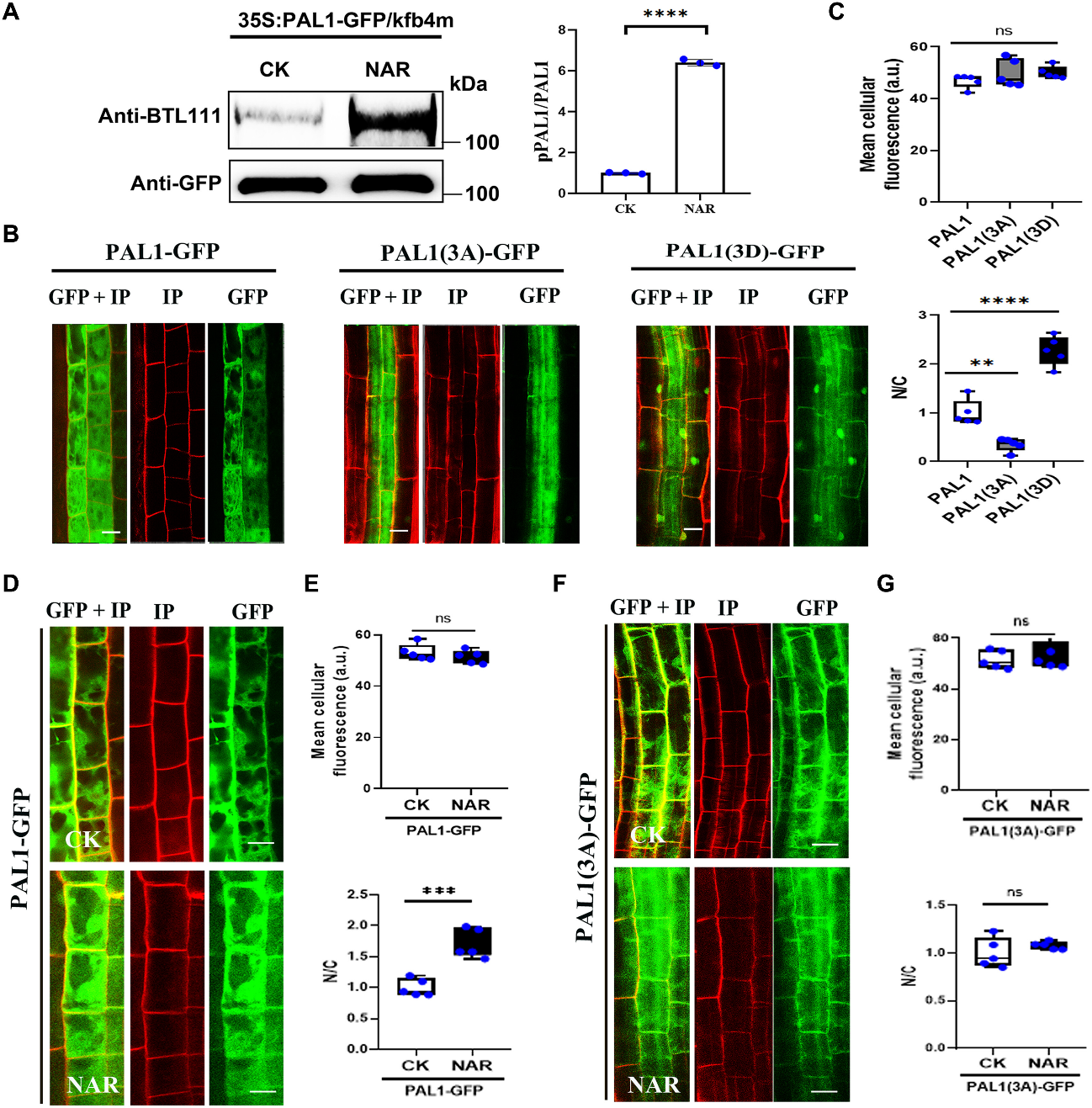
图2. 磷酸化诱导PAL入核
双重刹车机制:空间隔离+转录抑制
PAL进入细胞核后,会发生什么?研究团队揭示了一个精巧的“双重负反馈”机制:
- 空间隔离效应:PAL进入细胞核后,胞质中有效酶浓度下降,整体酶活显著降低;
- 转录干扰效应:核内PAL与MBW转录复合体核心组分TT8发生互作,破坏TT8与MYB75之间的结合,抑制CHS、CHI、F3H、FLS、DFR等黄酮关键基因表达。
该机制形成了“代谢物诱导—PAL磷酸化—核转位—双重抑制”的负反馈环路,实现黄酮生物合成的精细调控。
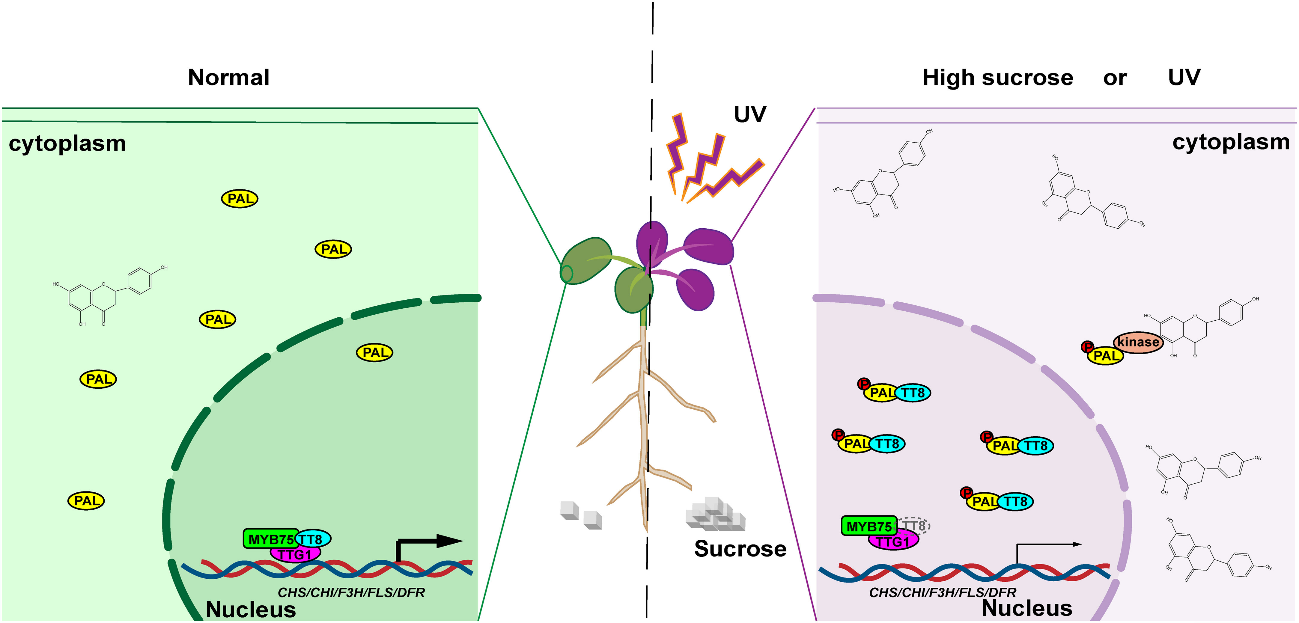
图3. PAL对类黄酮生物合成的动态调控模型
总结与展望
该研究首次揭示了PAL蛋白作为“代谢酶+信号整合器”的双重身份,这一发现不仅改写了人们对PAL蛋白功能的传统认知,更提出了代谢酶核定位参与转录调控的新范式,为理解植物特殊代谢的精细调控网络提供了全新视角。
中国科学院深圳先进技术研究院博士生孙林慧、助理研究员杨自凤及已出站博士后单晓彤(目前就职于东北师范大学)为该论文共同第一作者。中国科学院深圳先进技术研究院定量合成生物学全国重点实验室、合成基因组学研究中心赵乔研究员为该论文通讯作者,助理研究员王楠及博士生刘子乐也参与了数据分析与论文撰写。研究过程中,中国科学院深圳先进技术研究院定量合成生物学全国重点实验室、材料合成生物学研究中心高翔研究员和美国加利福尼亚大学伯克利分校谷杨楠教授给予了重要支持与专业指导。相关工作得到国家自然科学基金、广东省合成基因组学重点实验室、深圳市合成基因组学重点实验室、深圳合成生物学创新研究院等项目支持。
