JACS | 江寅迪/古阳实现植物螺环氧化吲哚生物碱的集群式生物合成
螺环氧化吲哚生物碱是一类结构复杂、生物活性多样的天然产物,具有显著的抗癌、抗高血压、抗炎等药理活性。然而,这类化合物在天然植物中含量极低,传统化学合成方法效率低下、成本高昂,难以满足药物开发和工业生产的需求。如何高效、可持续地生产这些天然产物,一直是该领域亟待解决的关键科学问题。
近日,中国科学院深圳先进技术研究院江寅迪研究员团队和周佳海客座研究员团队古阳副研究员合作,在国际期刊Journal of the American Chemical Society上发表了题为"Collective Biosynthesis of Plant Spirooxindole Alkaloids through Enzyme Discovery and Engineering"的最新研究成果。他们通过酶挖掘和蛋白工程相结合的策略,成功破解了植物螺环氧化吲哚生物碱的完整生物合成途径,并实现了12种四环和五环螺环氧化吲哚生物碱的集群式生物合成。

文章上线截图
(文章链接:https://pubs.acs.org/doi/10.1021/jacs.5c02990)
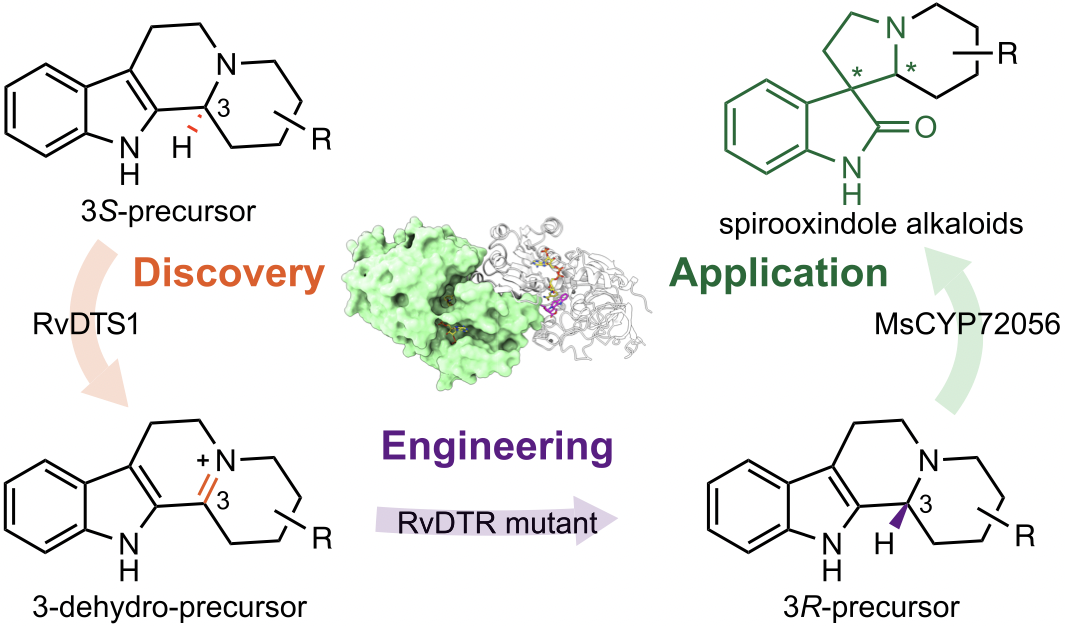
图1. 通过酶挖掘和蛋白工程,实现了螺环氧化吲哚生物碱的集群式生物合成
螺环氧化吲哚生物碱广泛存在于夹竹桃科、钩吻科和茜草科等植物中,具有独特的螺环结构和多样的生物活性。合成化学家们已成功开发出多种立体专一性合成策略来制备单个螺环氧化吲哚骨架,并建立了针对共同中间体的集群式全合成策略,能够同时获得多种结构相关螺环氧化吲哚生物碱。集群式全合成策略借鉴了生物合成的概念,然后利用生物合成酶来生产多种结构相关天然产物,也就是集群式生物合成,却面临两个核心挑战:首先,螺环氧化吲哚生物碱的生物合成途径仍然没有完全阐明;其次,生物合成酶往往表现出狭窄的底物范围,缺乏化学试剂那样的广泛适用性,严重限制它们在天然产物集群式生物合成中的应用。
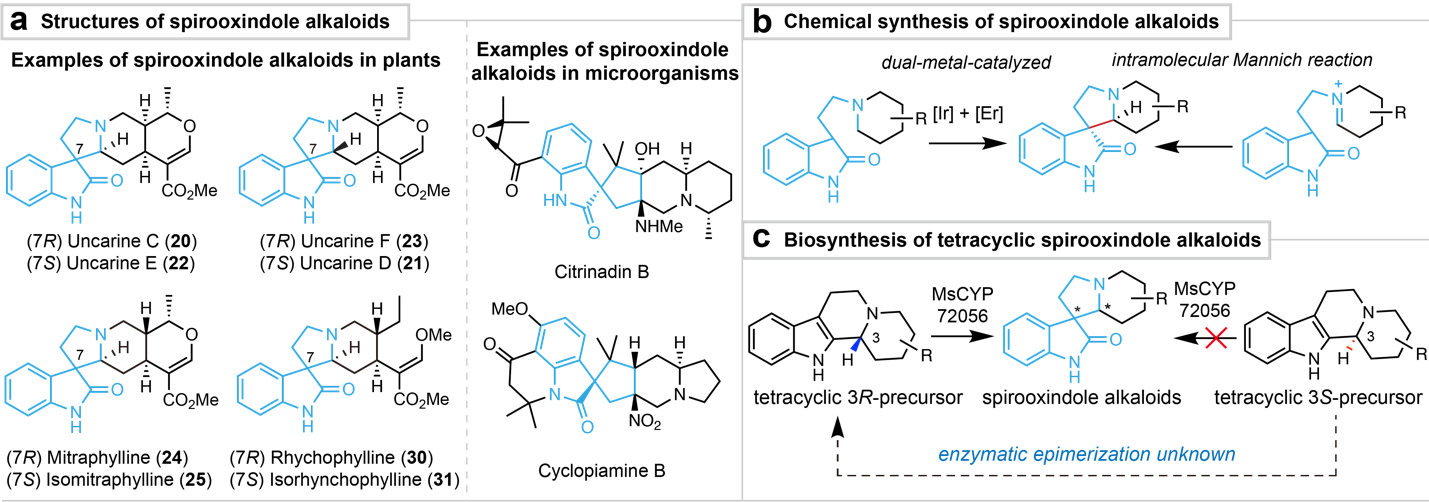
图2. 螺环氧化吲哚生物碱的化学结构、化学合成以及生物合成
螺环氧化吲哚生物碱生物合成酶的发现
为了实现螺环氧化吲哚生物碱的集群式生物合成,研究团队首先从药用植物萝芙木(Rauvolfia verticillata)中成功鉴定了两个关键酶:黄素依赖性氧化酶RvDTS1和中链脱氢酶RvDTR。这两个酶能够协同工作,将3S-四氢鸭脚木碱(5)通过连续的氧化和还原反应,立体专一性地异构化为3R-阿枯米精(6)。随后,前期发现的细胞色素P450酶MsCYP72056对3R构型的前体化合物进行氧化重排,最终形成四个五环螺环氧化吲哚天然产物Uncarines C, D, E, 和F。

图3. 螺环氧化吲哚生物碱生物合成酶的挖掘
酶工程扩展底物范围实现集群式生物合成
野生型RvDTR酶的底物特异性较强,限制了其在集群式生物合成中的应用。研究团队通过结构指导的蛋白工程技术扩展了RvDTR的底物识别范围。他们构建了RvDTR与底物复合物的三维结构模型,并通过定点突变策略成功改造了酶的活性位点。其中,T123G突变破坏了野生型酶中的氢键网络,增加了门控环的柔性,从而将RvDTR从底物特异性酶转变为具有广泛底物范围的催化剂。利用工程改造后的酶系统,研究团队成功实现了12种四环和五环螺吲哚天然产物的集群式生物合成,包括帽柱木菲碱(24)、异帽柱木菲碱(25)、钩藤碱(30)和异钩藤碱(31)等重要生物碱。这种集群式生物合成策略相比传统的单一产物生物合成方法具有显著优势,能够从共同的中间体高效生产多种结构相关的天然产物。
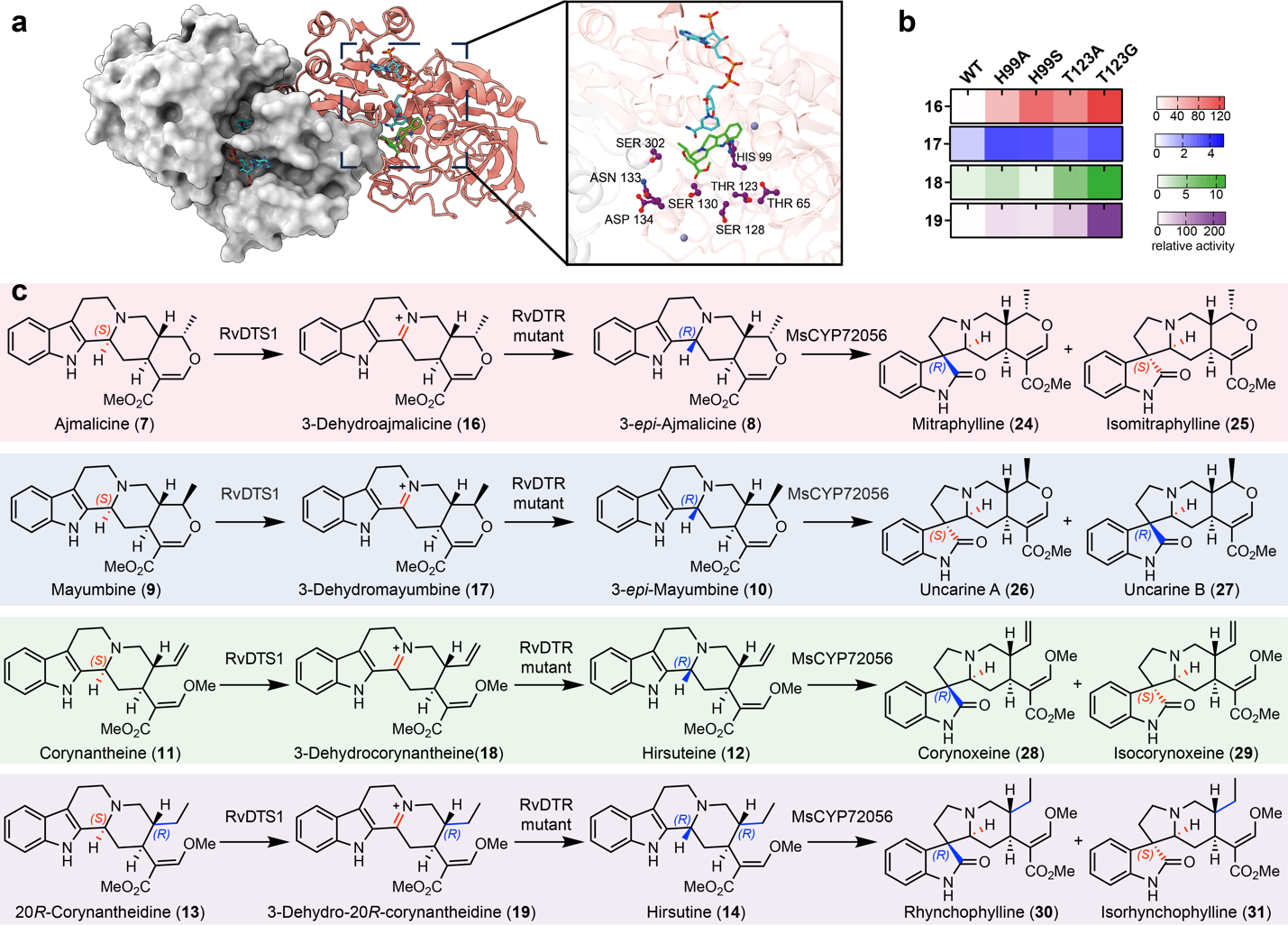
图4. RvDTR的蛋白工程改造扩展底物范围,实现螺环氧化吲哚天然产物的集群式生物合成
该研究不仅阐明了植物螺环氧化吲哚生物碱的生物合成途径,更重要的是建立了一个通用的集群式生物合成平台。这种将酶挖掘与蛋白工程相结合的策略为其他复杂天然产物家族的可持续生产提供了重要参考。研究成果在烟草和酵母两个异源宿主系统中都得到了验证,展现了良好的工业化应用前景。
中国科学院深圳先进技术研究院江寅迪研究员和周佳海客座研究员团队古阳副研究员为论文通讯作者,江寅迪团队助理研究员储丹妮为文章第一作者。该研究得到国家重点研发计划、深圳市科技重大专项以及深圳合成生物学创新研究院等多个项目的支持。
