
2024年5月8日,中国科学院深圳先进技术研究院合成生物学研究所、深圳合成生物学创新研究院的甘海云研究员课题组,美国明尼苏达大学Hormel研究所的于传贺教授和四川大学华西医院生物治疗全国重点实验室、疾病分子网络前沿科学中心的韩俊宏教授课题组在PNAS(Proceedings of the National Academy of Sciences)发表了题为“DNA聚合酶δ调控亲代组蛋白传递到DNA复制的滞后链上(DNA polymerase delta governs parental histone transfer to DNA replication lagging strand)”的文章,该研究发现聚合酶δ(Pol δ)在DNA复制期间作为关键伴侣蛋白,将亲代组蛋白传递到滞后链上,确保携带亲代组蛋白翻译后修饰的表观遗传信息能够忠实地传递给子代细胞。这一发现揭示了Pol δ在复制DNA滞后链时促进亲代组蛋白遗传的精细过程。Pol δ被认为参与DNA损伤修复过程,但其功能未知,这提示组蛋白回收可能参与DNA损伤修复过程。
文章上线截图
文章链接:https://www.pnas.org/doi/10.1073/pnas.2400610121
在前不久的3月8日,同样由甘海云研究员课题组及美国明尼苏达大学Hormel研究所的于传贺教授在NAR(Nucleic Acids Research)发表题为“亲代组蛋白传递缺陷通过增加游离组蛋白的浓度来降低同源重组的频率(Defective transfer of parental histone decreases frequency of homologous recombination by increasing free histone pools in budding yeast)”的文章,该研究明确了亲代组蛋白H3-H4四聚体传递遭到破坏时产生的遗传和表观遗传结果。这一发现揭示了DNA复制过程中亲代组蛋白正确传递不仅对维持染色质结构的稳定性至关重要,而且任何由于亲代组蛋白传递缺陷导致的同源重组活性降低都可能对细胞健康产生不利影响。

文章上线截图
文章链接:https://doi.org/10.1093/nar/gkae205
DNA复制和组蛋白传递是生物体内两个紧密相连的过程,它们共同确保了遗传信息的准确传递和生物体的正常运作。在DNA复制过程中,复制叉前的亲代核小体结构需要被解组装,同时,亲代核小体上的组蛋白会被传递到复制叉后面新生成的子链DNA,包括前导链(leading strand)和滞后链(lagging strand)上重新组装形成核小体,实现表观遗传信息的传递和继承。近年来,甘海云研究员与合作者通过开发能特异性检测DNA复制过程中前导链和滞后链结合蛋白的技术 (enrichment and sequencing of protein-associated nascent DNA,eSPAN),发现DNA聚合酶Pol ε在合成DNA的同时,其亚基Pole3和Pole4还负责将亲组蛋白传递到前导链(Science, 2018)。Mcm2(Mcm2-7解旋酶的一个亚基)通过Pola将亲组蛋白传递到复制DNA的滞后链(Molecular Cell, 2018)。但MCM2本身位于Leading链上,Polα只能合成RNA引物和大约30nt的DNA序列,表明仅凭目前已知的通路无法完成Lagging上的组蛋白回收,这一直成为科研工作者们探索的谜题。
甘海云研究员课题组及其合作者经过大量的筛选和实验验证,最后发现滞后链DNA聚合酶δ的非必需亚基Pol32的缺失,会导致复制过程中亲代组蛋白H3-H4主要传递到前导链。进一步的生化分析表明,Pol32在体内和体外都能与组蛋白H3-H4结合(图2)。
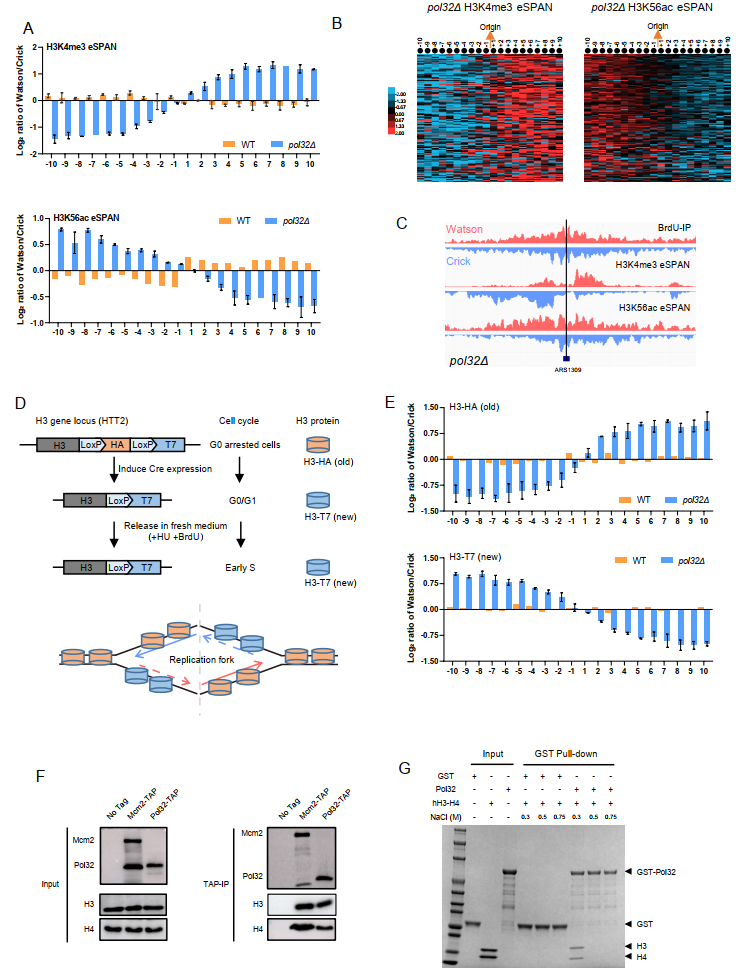
图2. Pol32 介导亲组蛋白H3-H4传递到滞后链
研究者还通过将Mcm2内组蛋白H3-H4结合域突变,发现Pol32与亲代组蛋白H3-H4的相互作用遭到破坏,这进一步证实了Mcm2和Pol32两者之间存在的紧密联系。综合这些发现,DNA聚合酶δ亚基Pol32被鉴定为Mcm2下游的关键组蛋白伴侣,它能够介导DNA复制过程中亲代组蛋白向滞后链的传递(图3)。这一发现不仅揭示了亲代组蛋白传递机制的一个关键环节,还为未来关于遗传信息和表观遗传信息传承的研究提供了新的方向。

图3. Mcm2,H3-H4以及Pol32在复制叉处的互作
中国科学院深圳先进技术研究院的助理研究员田聪聪、助理研究员周嘉琦、研究助理张紫微和四川大学的博士生张琴、美国明尼苏达大学的博士后贾静为论文的共同第一作者。该研究获得国家合成生物学重点研发计划,国家自然科学基金重大项目,中国科学院战略性先导科技专项,国家自然科学基金面上项目、青年项目、广东省自然科学杰出青年基金、深圳合成生物学研究创新研究院科研计划和深圳市医学研究基金等多个项目的支持。
专家点评
深圳大学朱卫国教授
近年来研究发现亲代组蛋白的遗传对子细胞的表观重建、分化特征维持、乃至个体发育都至关重要。DNA复制偶联的亲代组蛋白传递保证了表观基因组的稳定遗传,甘海云和合作者此前发现解旋酶亚基MCM2和DNA聚合酶polα负责亲代组蛋白向滞后链的传递。然而,MCM2本身位于前导链上,polα作为引物酶只能合成滞后链复制所需的RNA引物和大约30nt的DNA序列,很显然无法完成整个滞后链的亲代组蛋白回收。这个问题也一直成为谜题。这项研究甘海云领衔的团队发现在酵母细胞中DNA聚合酶polδ的非必需亚基pol32可以作为组蛋白伴侣将亲代组蛋白至滞后链,该研究完成了DNA复制偶联的组蛋白回收通路的最后一块拼图,完善了DNA复制偶联组蛋白回收的理论,把DNA复制和染色质复制终于统一到了一起。另外,有证据表明polδ可能参与DNA损伤修复过程,甘海云和合作者最近的NAR文章也发现亲代组蛋白传递缺陷会影响同源重组频率。这些研究不仅填补了先前对组蛋白回收机制的认识空白,还为研究DNA损伤修复过程中的染色质修复提供了新的视角。
PI与课题组简介
甘海云博士,中国科学院深圳先进技术研究院合成生物学研究所研究员,博士生导师。近五年来研究成果发表在Science、Nature Medicine、Nature Genetics、Molecular Cell、Nature Communications、Genes & Development、PNAS、eLife、The EMBO Journal、Nucleic Acids Research等知名期刊,累计引用超过3400次。
课题组主要研究方向为利用系统生物学、合成生物学以“干湿”实验结合的模式研究表观基因组信息的传递机制以及其在肿瘤发生和耐药性产生、全能性细胞(2C)、细胞衰老、染色体外DNA(ecDNA)、合成表观重构、DNA复制起始分子复合物、人工细胞等的表观遗传调控机制。
课题组现招聘有表观基因组学、合成生物学、生物信息学、肿瘤生物学、细胞生物学等任一相关研究背景博士后1-2名,研究助理2-3名,欢迎志同道合的朋友投送简历至hy.gan@siat.ac.cn,简历及邮件标题注明“应聘岗位-学校名称-专业-姓名”。