
微生物具有生物合成海量活性天然产物的能力,这些天然产物一直是人类药物开发的主要来源,与人类健康和社会安全可谓密切相关,同时也在农业、畜牧业、食品行业等领域发挥至关重要的作用。微生物天然产物的生物合成过程错综复杂,受自身和环境因素影响巨大。特别是在实验室条件下,大量天然产物生物合成基因处于“沉默”状态,它们的产物被称为微生物“生命暗物质”(Nature 2015;Nature Reviews Drug Discovery 2023)。如何有效激活并挖掘这些微生物“生命暗物质”一直是限制新天然产物发现的瓶颈, 也是该领域世界性的挑战。目前,该领域的研究主要集中在通过对单个菌株的遗传物质、生活环境、或者代谢物质等进行调控,进而在实验室条件下激活并发掘微生物“生命暗物质”。然而,天然产物的合成和调控过程复杂、不同产生菌株的生理和代谢存在差异、菌株培养和遗传操作周期长,这些因素大大限制了这些手段对该领域的推动作用。随着基因测序技术的普及,大量的基因组数据和逐渐成熟的基因组分析技术有望绕过繁冗的改造工序,突破菌株个体的差异性,为研究天然产物合成的普适规律和开发改造工具提供思路。
北京时间4月12日,罗小舟/Jay D. Keasling/唐啸宇课题组合作在《Nature Metabolism》期刊上发表题为Elucidation of Genes Enhancing Natural Product Biosynthesis Through Co-evolution Analysis的研究论文,并在同一期发表题为Co-evolved Genes Improve the Biosynthesis of secondary metabolites的研究简报。研究团队通过共进化分析在链霉菌属鉴定了与聚酮合酶共进化597个基因,这些基因分别隶属于转录、转运、辅酶、脂肪酸合成、金属离子转运等不同功能家族分类。研究以位于“辅酶”家族中的吡咯喹啉醌(PQQ)基因为例在多株放线菌中进行应用,发现导入PQQ生物合成途径可以显著提升链霉菌的天然产物产量,并产生了多种具有潜在药物潜力的新化合物,对于开发新型抗生素以及提高天然产物产量具有重要意义。

文章上线截图
文章链接:https://www.nature.com/articles/s42255-024-01024-9
链霉菌是已知的天然产物生物合成基因簇最丰富的微生物之一,广泛分布于土壤、水源以及植物表面。由于自然环境中营养匮乏且无运动功能,链霉菌进化出大量次级代谢基因,以基因簇的形式存在,用以生产各种生物活性物质来抵抗外敌和抑制竞争对手。前期研究发现,链霉菌中编码的次级代谢基因簇明显多于其它物种,而其内部不同的属、不同的种之间编码次级代谢基因簇的能力差异也很大。因此, 在拥有更多次级代谢基因簇的链霉菌在长期进化过程中,为了维持该菌株合成多种次级代谢产物,这些物种基因组中可能也同时进化出了多种有利于各种次级代谢产物合成的基因。 寻找到这些拥有丰富的次级代谢基因簇的菌株(图1),并挖掘到这些共进化基因,将为拓展我们揭秘天然代谢“生命暗物质”的工具箱,也可以开发出改造链霉菌促进次级代谢产物合成和激活沉默基因簇的新方法。

图1 链霉菌属的系统进化及次级代谢基因簇分析。链霉菌被分为14个家族,其中家族12编码的PKS基因簇明显多于其它家族
基于此原因,该团队通过泛基因组分析技术寻找到与聚酮化合物基因簇共同进化的597个基因(图2),并在其中以辅酶吡咯喹啉醌(PQQ)合成的基因簇为例展开研究,推测PQQ在链霉菌的天然产物生物合成中中发挥关键作用。
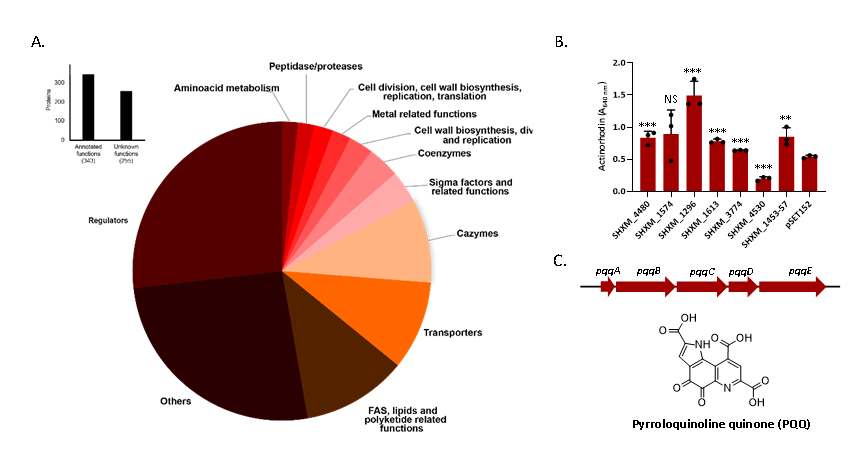
图2 597个共进化基因的分类(A)及功能表征(B、C)。(B)Coenzyme家族的基因对放线紫红素合成的作用;(C)吡咯喹啉醌(PQQ)基因簇和结构
该研究团队在11个链霉菌菌株和其他两个工业放线菌菌株中引入PQQ生物合成途径,发现这一改造显著提高链霉菌的天然产物产量,至少有16,385种代谢产物的生产得到了提高,其中包括36种已知天然产物(图3)。这些天然产物具有广泛的应用价值,包括抗菌剂、抗真菌剂、抗癌剂等。

图3 导入PQQ基因簇促进了多种已知天然产物的合成
除了增强天然产物的产量外,研究团队还观察到引入PQQ基因簇后,一些沉默的天然产物生物合成基因簇的转录活性上调。这意味着PQQ不仅可以直接影响已知天然产物的生物合成,还可能激活链霉菌中未被发现的潜在代谢途径,丰富了天然产物的种类和多样性。进一步的实验也验证了此观点,在引入PQQ基因簇的链霉菌菌株中发现了一些新的代谢产物,其中一些具有潜在的抗生素活性,甚至对临床感染菌株具有活性(图4)。这为新型抗生素的发现和未来药物开发提供了重要线索和候选化合物。
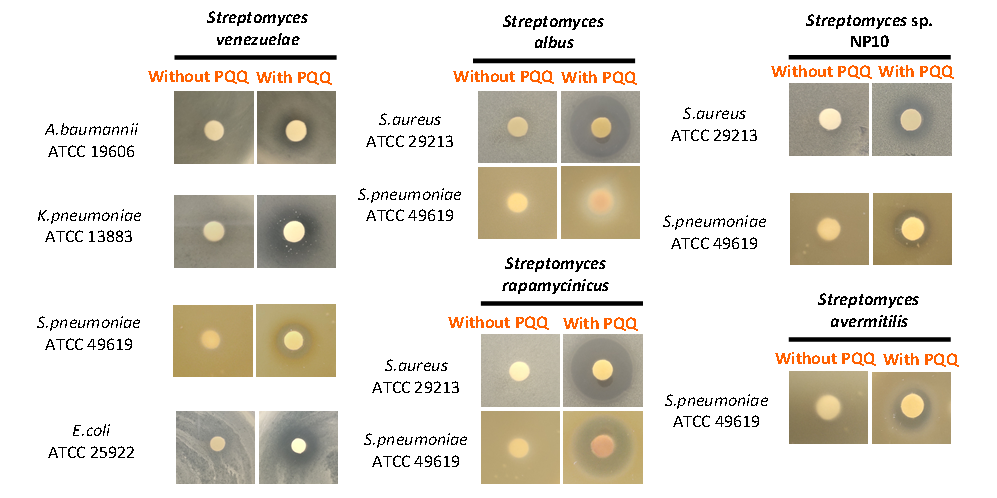
图4 导入PQQ基因簇激活了未知的抗感染天然产物的合成
此外,该研究通过深入的蛋白质组和代谢组分析,揭示了PQQ提升天然产物合成效率的机理。研究发现,PQQ基因簇转入后可提升ATP水平并提高关键辅因子比率,同时提升甘油三酯降解产生关键前体乙酰-CoA,因此提升了多种天然产物的合成。
目前,在链霉菌中用于提升天然产物产量的工程策略主要有两种:一是通过代谢工程来增强前体生物合成途径或删除竞争途径;二是改造调控因子以增强合成途径基因的表达水平。然而,鉴于天然产物生产者和生物合成途径的广泛多样性,迄今为止仍鲜有通用策略来提高不同的天然产物的产量。该研究利用泛基因组分析技术系统分析整个链霉菌属的基因组,以自下而上的方式寻找普适的改造方法,绕过了传统基于机理研究所耗费的时间与人力成本,为在不同的植物和微生物物种中开发不同类型的天然产物的改造方法提供新的思路,加速了认知天然产物合成过程的“暗物质”的步伐。
中国科学院深圳先进院合成生物学研究所研究员罗小舟、美国加州大学伯克利分校教授Jay D.Keasling及深圳湾实验室化学生物学研究所研究员唐啸宇为本文的通讯作者,助理研究员王欣然、研究助理陈宁辛、丹麦技术大学 Pablo Cruz-Morales 研究员为文章共同第一作者。上海交通大学的白林泉教授和华中科技大学的孙宇辉教授也对研究做出了贡献。该工作得到了国家重点研发计划、国家自然科学基金委、深圳市科技计划项目、深圳市医学研究专项等多个项目的资助以及深圳合成生物学创新研究院等平台的支持。同时,感谢中国科学院深圳先进院合成生物学研究所的科研助理魏珍琴在项目实施过程中协助组织会议讨论等支撑工作。
专家点评:
中国科学院院士邓子新:
通过共进化策略揭示了增强天然产物生物合成的关键基因。这一成果体现了以合成生物学为牵引,汇聚生物信息学、微生物遗传学、基因组和代谢组学等多个学科,为合成生物学领域跨学科交叉与合作提供了新的成功范例。
微生物天然产物的生物合成过程异常复杂和精巧,并受到自身和环境因素的共同影响。在实验室条件下,许多微生物天然产物生物合成基因往往处于沉默状态,这些“暗物质”成为了有待深入发掘的天然产物新源泉。该团队在国家重点研发计划合成生物学重点专项的支持下,通过共进化分析,在链霉菌属中鉴定出了与聚酮合酶共进化的597个基因,并发现引入其中的PQQ生物合成途径,显著提高了链霉菌的天然产物产量,产生了多种具有药物潜力的新化合物,为新药发现提供了重要线索和物质基础。
值得注意的是,该研究采用了泛基因组分析技术,绕过了繁琐的改造工序,突破了菌株个体的差异,为研究天然产物生物合成的普适性规律提供了新思路。国家重点研发计划合成生物学领域咨询专家、中国科学院院士邓子新指出:“这项成果不仅激发了我们对重启微生物天然产物‘暗物质’生物合成的共同兴趣,也为合成生物学在药物研发等领域的应用提供了新的策略。我期待着未来能看到更多类似的研究成果,为人类健康和社会发展做出更大的贡献。”
南京大学生科院副院长戈惠明:
天然产物是小分子药物的主要来源。尽管基因组测序和生物信息学分析已经暗示大量“沉默”生物合成基因簇的存在,然而如何在实验室条件下激活这些“生命暗物质”是该领域长期以来面临的一项重大挑战。在这项研究中,来自深圳先进院的罗小舟、Jay Keasling以及深圳湾实验室的唐啸宇联合研究团队,利用泛基因组分析方法,搜寻与天然产物基因簇连锁共进化的基因,通过实验揭示了吡咯喹啉醌辅因子(PQQ)与聚酮基因簇表达密切相关,并进一步阐明过表达PQQ基因簇激活大量新天然产物分子合成的普适性。这项研究的独特视角和创新观点不仅为新天然产物的挖掘提供了新的途径,还有助于提高现有重要天然产物的产量。
值得注意的是,这项研究不仅关注天然产物的合成,还强调了基因之间的相互作用和共同进化对于生物合成过程的影响。这种综合性的研究方法有助于我们全面理解天然产物生物合成的复杂性,为未来设计更高效的生物合成途径提供了新的思路和策略。总的来说,这项研究推动了天然产物挖掘和天然产物合成生物学的发展,为我们深入理解天然产物的生物合成过程提供了全新的视角和方法。