
11月14日,中国科学院深圳先进技术研究院合成生物学研究所罗小舟研究员和Jay. D. Keasling教授课题组在Nature Synthesis上发表题为“Engineering yeast for de novo synthesis of jasmonates”的文章。该研究针对现阶段植物激素茉莉素在生产上面临的化学合成难度大、植物提取得率低等挑战,提出在酿酒酵母中重构茉莉素的生物合成途径,建立微生物细胞工厂以实现高效和绿色生产,为茉莉素在农业及化妆品行业的规模化应用铺平道路。

文章上线截图
文章链接:https://www.nature.com/articles/s44160-023-00429-w
茉莉素(jasmonates)是茉莉酸及其衍生物茉莉酸甲酯、茉莉酸异亮氨酸等的统称。作为植物的抗性激素,茉莉素在调节植物生长发育和逆境应答过程中有着举足轻重的作用,被广泛应用于增产提质、抗寒防冻、抵御虫害等。美国和日本等国家已将茉莉素投入到农业生产上,在改善苹果、葡萄、柑橘等作物的果实品质和防御能力上卓有成效,茉莉素正凭借其强大的抗病虫害能力跻身于生物农药主力军的行列。此外,茉莉素还因其特殊的香味,在化妆品领域占据一席之地。素有“合成茉莉”之称的二氢茉莉酮酸甲酯作为茉莉素衍生物,是香料界使用最多的产品之一,最早应用于迪奥的“Eau Sauvage”香水,现被用于几乎所有类型的香水中。一份来自于QYResearch的调研报告显示:2025年,全球二氢茉莉酮酸甲酯的市场规模将达12亿元人民币。茉莉素市场未来可期。
然而,茉莉素主要来源于传统的植物提取,但植物中的低含量和萃取过程的繁琐在不同程度上导致生产成本攀升;复杂的立体构型,又给化学全合成带来不少挑战,生产上的种种困境严重限制了茉莉素的规模化应用。
合成生物学的发展使得天然产物的异源生产成为可能。自1962年从素馨花中首次发现并分离茉莉酸甲酯以来,科学家一直致力于茉莉素生物合成通路的解析,完整的合成途径在2012年问世。茉莉素在植物中的合成过程较为复杂,通路长,酶促类型多样,还涉及中间产物在不同细胞器间的转运:磷脂酶先将α-亚麻酸(α-LeA)从叶绿体膜上释放;α-LeA在叶绿体内,由多酶复合体催化形成12-氧代-植物二烯酸(OPDA);OPDA在过氧化物酶体中,经过3轮β-氧化生成茉莉酸(JA);JA在细胞质中被转化为下游衍生物茉莉酸甲酯(MeJA)、茉莉酸异亮氨酸(JA-Ile)等。公认安全的酿酒酵母因含有多种细胞器,被该团队优先选择为茉莉素异源从头合成的微生物底盘。合成途径的复杂度为重构工作带来不少挑战,其中,在酵母中找寻适合中间体α-LeA和OPDA合成的场所,是途径重构首要解决的难题。
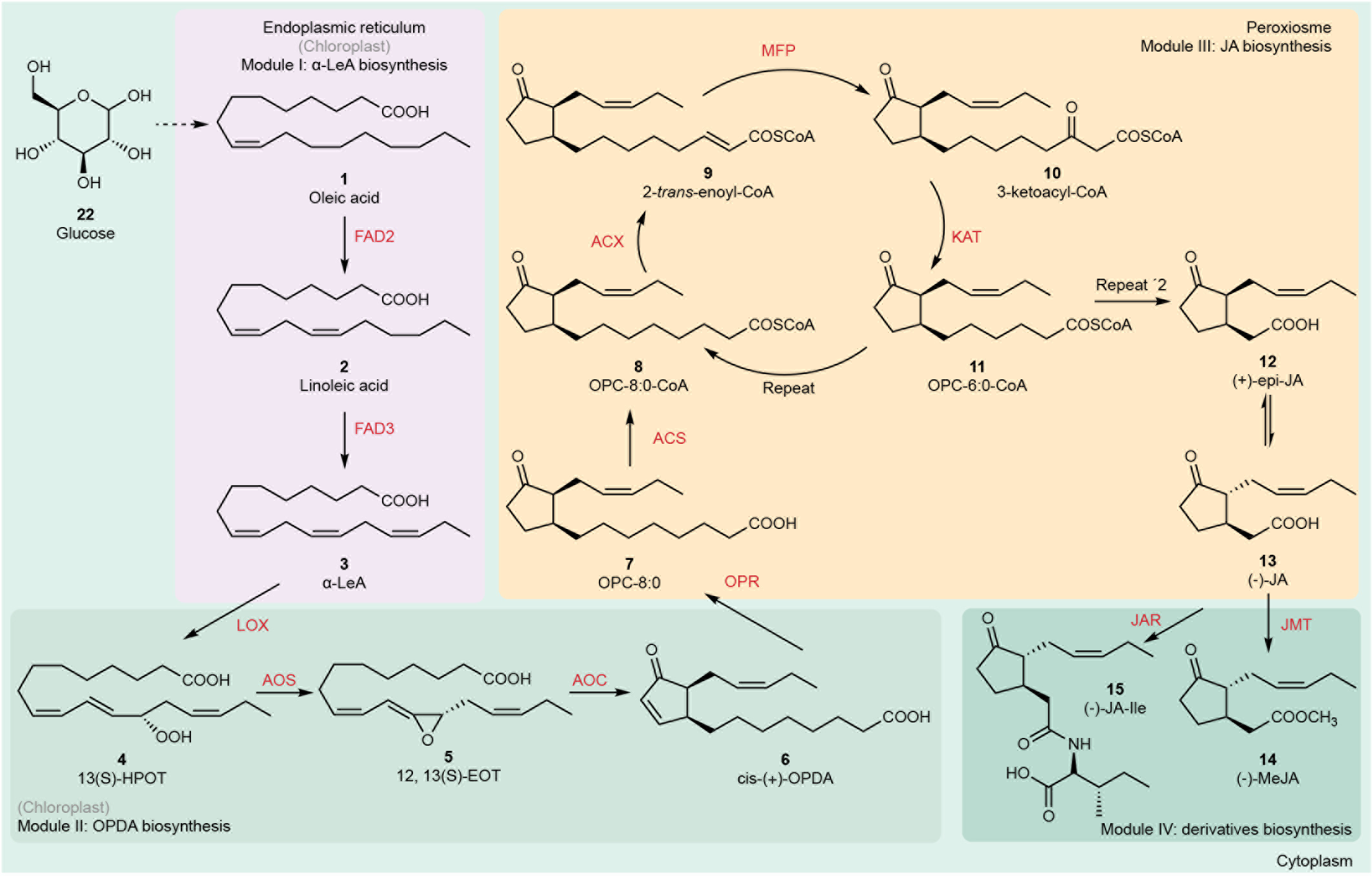
图1:茉莉素的生物合成通路。根据产物类型和合成场所的不同,将茉莉素在酵母中的重构途径分为4个模块:模块1在内质网中合成α-LeA;模块2在细胞质中合成OPDA;模块3在过氧化物酶体中合成JA;模块4在细胞质中合成MeJA和JA-Ile。灰色代表相应化合物在植物中的合成场所。
在该研究中,研究团队首先在酵母的内质网中合成α-LeA。α-LeA在植物的叶绿体中被合成,而酵母缺少叶绿体结构;酵母虽不能从头合成α-LeA,却可以在内质网中合成α-LeA的前体。受启发于此,该团队尝试在酵母的内质网中合成α-LeA。通过在酿酒酵母中引入克鲁维酵母来源的FAD,实现α-LeA在酵母的从头合成(图2A),但α-LeA的产量仅0.7 mg/L,远不够进行下游转化。共聚焦实验表明,相关基因均成功定位在内质网(图2B)。同时,研究人员还基于改造自由脂肪酸的代谢通路(图2C),将α-LeA的产量提升至51.2 mg/L(图2D)。
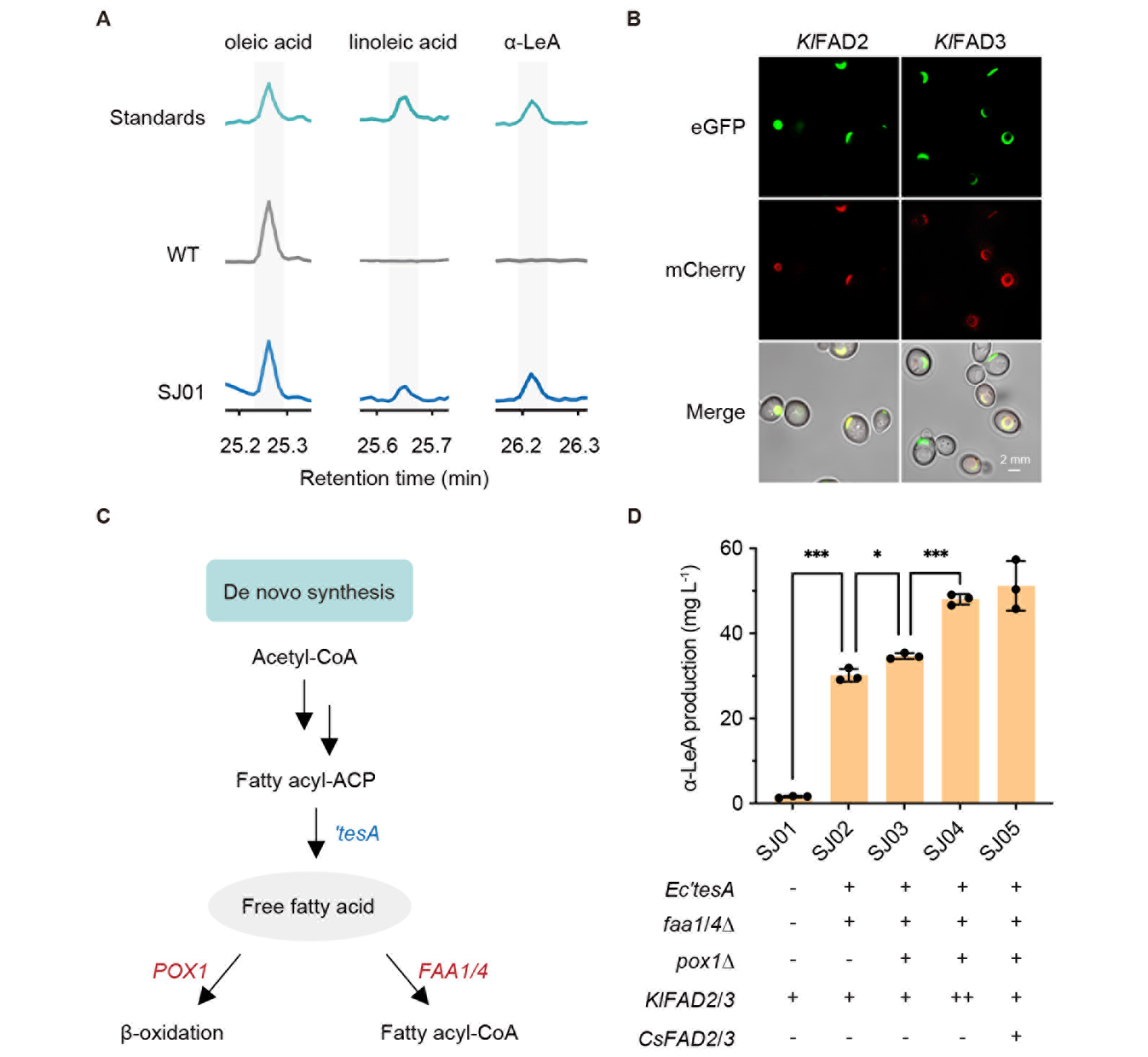
图2:在酵母内质网中合成α-LeA。
其次,在酵母的细胞质中合成OPDA。OPDA在植物的叶绿体中被合成,同样需要在酵母中寻找适合OPDA合成的场所。细胞质和过氧化物酶体是潜在的候选选项:若在细胞质中合成OPDA,后续需要OPDA转运进过氧化物酶体完成下游转化;若在过氧化物酶体中合成OPDA,则需要底物α-LeA先行转运至过氧化物酶体。考虑到α-LeA在过氧化物酶体中被降解的可能性,该团队尝试将OPDA合成途径(LOX、AOS和AOC)定位至酵母的细胞质中。首先对不同来源的LOX进行活性筛选(图3A)和组合表达,将中间体13-HPOT的产量提升至10.8 mg/L(图3B)。继续引入AOS和AOC,成功实现OPDA的生产,产量4.9 mg/L(图3C和3D)。共聚焦实验表明,相关基因均成功定位在酵母的细胞质(图3E)。
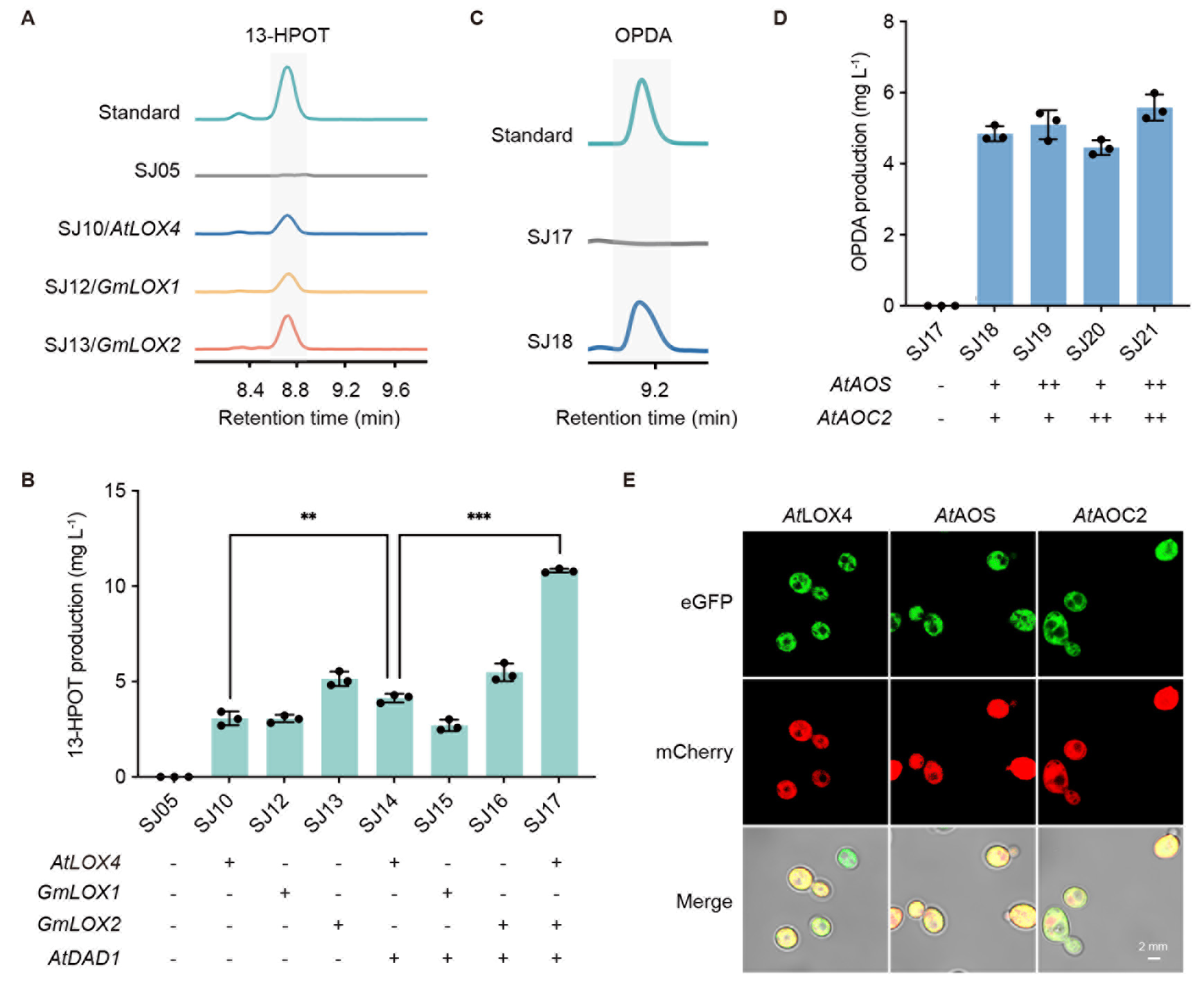
图3:在酵母细胞质中合成OPDA。
紧接着,在酵母的过氧化物酶体中合成JA。鉴于植物和酵母在β-氧化过程上的相似性,该研究直接模仿植物中JA的合成过程,在酵母中引入保留了自身过氧化物酶体定位肽的相关酶(OPR、ACS、ACX、MFP和KAT),在过氧化物酶体中成功实现JA的合成,产量达9.6 mg/L(图4A和4B),进一步饲喂底物α-LeA,JA的产量可达19.0 mg/L。
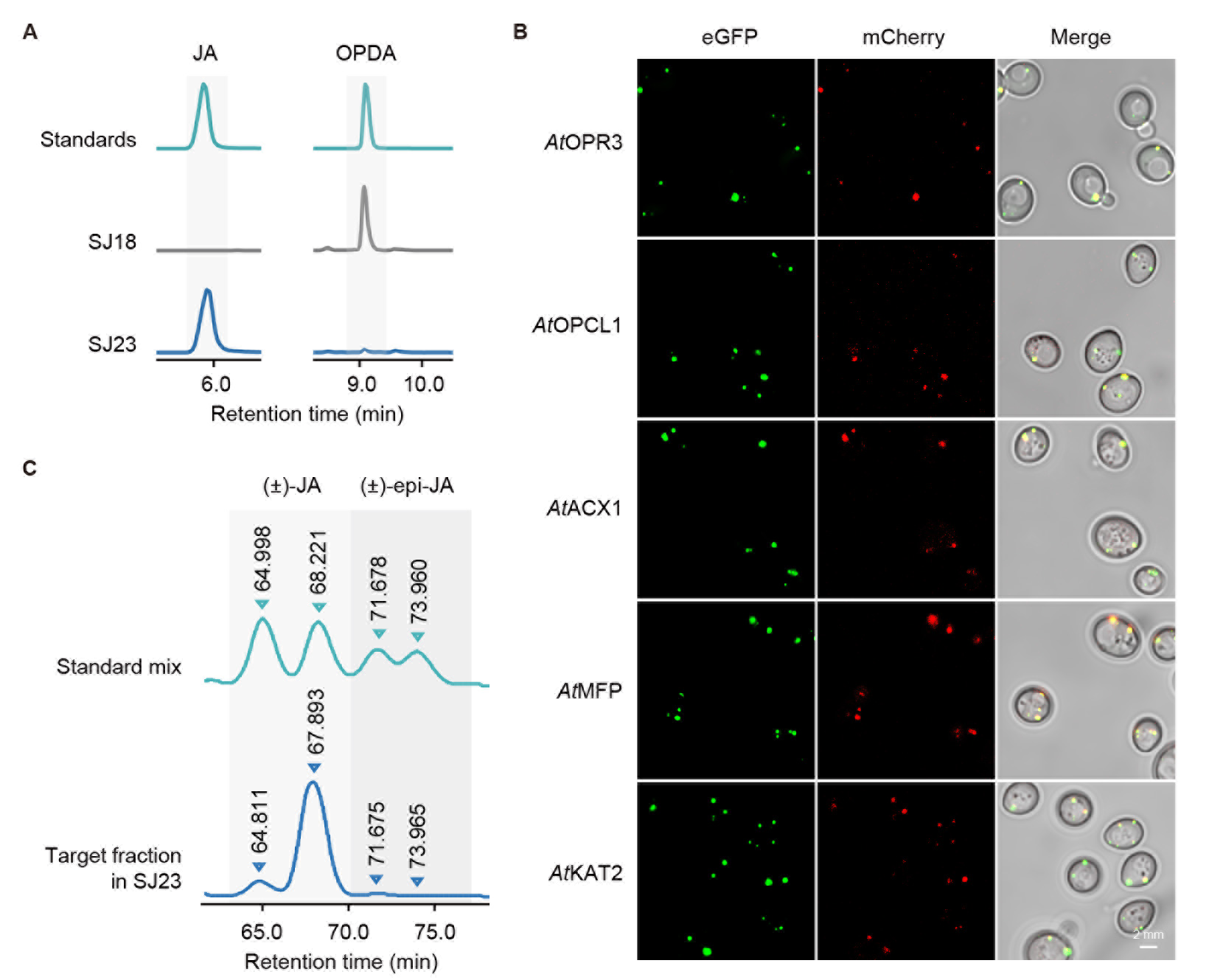
图4:在酵母过氧化物酶体中合成JA。
最后,在酵母的细胞质中合成MeJA和JA-Ile等衍生物。在产JA的酵母底盘中引入JMT以合成MeJA,产量3.1 mg/L(图5A和5B);引入JAR合成JA-Ile,产量7.0 mg/L(图5C和5D)。
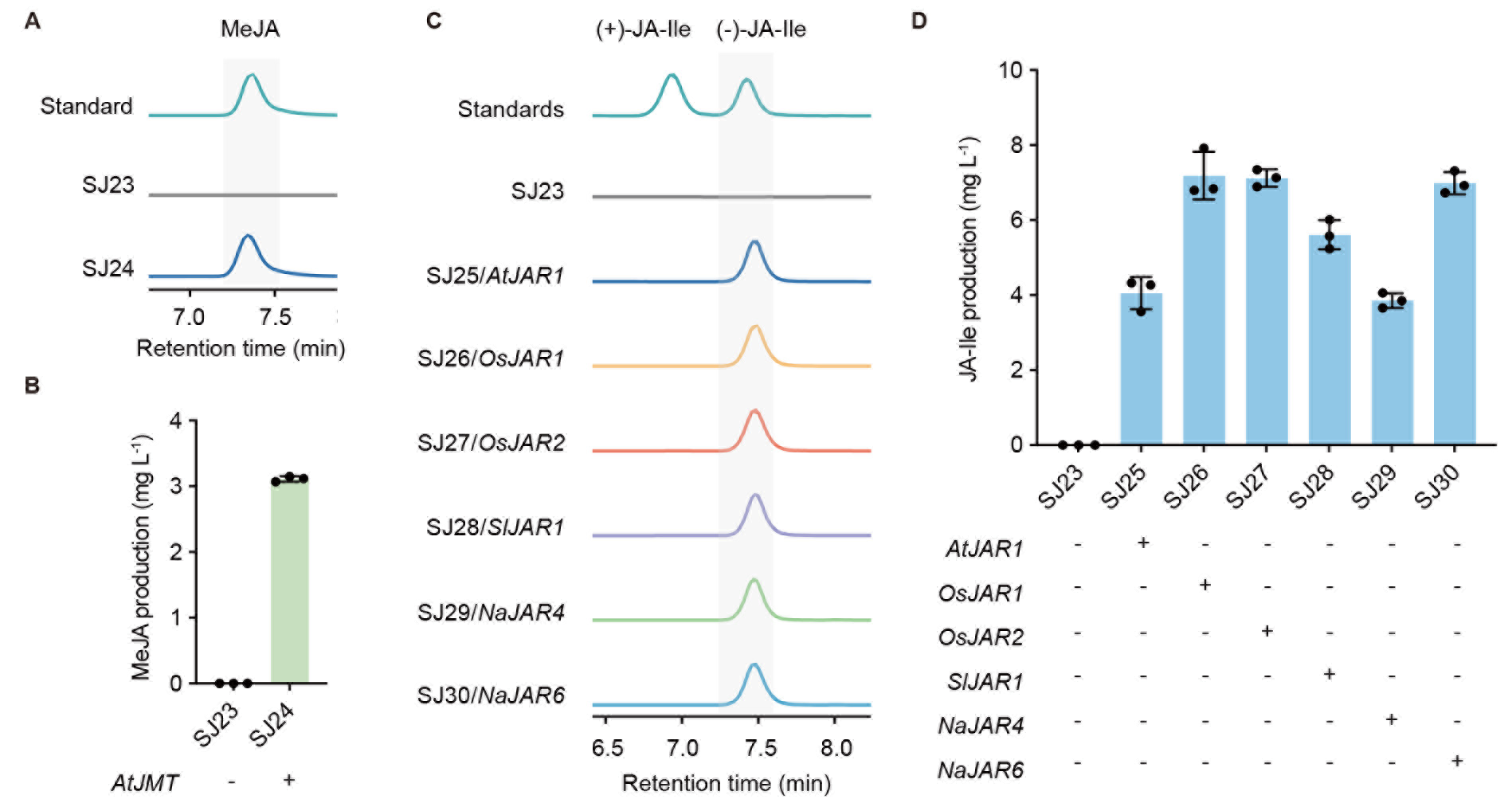
图5:在酵母细胞质中合成MeJA和JA-Ile。
至此,研究团队成功建立了植物激素茉莉素的酵母细胞工厂。相较于传统的植物提取,此法在生产上不受时令限制、可规模化放大,为茉莉素的高效和绿色生产提供了重要的参考。
中国科学院深圳先进院合成生物学研究所罗小舟研究员、Jay. D. Keasling教授和汤红婷副研究员为本文的共同通讯作者,团队成员汤红婷副研究员、林淑敏和邓吉良为文章并列第一作者。该研究获得国家重点研发计划、国家自然科学基金委、广东省基础与应用基础研究基金委、深圳市科技计划及深圳合成生物学创新研究院等多个项目的支持。同时,感谢于涛研究员在脂肪酸代谢通路改造研究上的学术讨论和宝贵意见;感谢科研助理魏珍琴在项目实施过程中协助组织会议讨论;感谢化学与组学分析平台为本项目的色谱和质谱分析提供强大的硬件支撑。
罗小舟,深圳先进院合成生物学研究所研究员,博士生导师,合成生物化学研究中心执行主任、PI,深圳市合成生物研究重大科技基础设施副总工艺师,森瑞斯生物科技(深圳)有限公司创始人。2010年于新加坡南洋理工大学获得学士学位,2016年于美国圣地亚哥斯克里普斯研究所获得化学专业博士学位(导师Peter G. Schultz院士),2016-2019于加州大学伯克利分校进行博士后研究(合作导师Jay D Keasling院士)。2019年加入中国科学院深圳先进技术研究院。先后入选国家重大人才工程(青年)专家、广东省杰青、深圳市优青、深圳市国家级高层次人才、2023南山十大杰出青年等。在 Nature, Nature Chemical Biology, Cell Chemical Biology, Nature Synthesis, PNAS, Angewandte Chemie等知名学术期刊上发表论文30余篇。课题组聚焦于合成生物学领域中生命体内生物化学过程相关研究,主要结合遗传密码扩充技术,酶的定向进化,基因挖掘和代谢工程等多种化学生物学方法,基于大数据机器学习及高通量自动化,深入研究多种不同类别的天然产物及其衍生物的生物全合成的方法,并利用合成生物学方法,将研究成果转化至制药、个性化治疗、新材料等领域。
课题组现长期诚聘生物、化学、生物信息学、生物医学工程等交叉学科背景,或有酶定向进化、机器学习、高通量筛选、天然及非天然化合物的生物全合成等研究背景的博士后,欢迎感兴趣的同志投递简历至邮箱xz.luo@siat.ac.cn。